Stress, irritabilité, nervosité, migraines, crampes… et si le magnésium faisait défaut ? Le magnésium Mg2+ est le deuxième cation le plus abondant du corps humain et intervient dans plus de 300 réactions enzymatiques. De nombreux symptômes peuvent témoigner d’un déficit en magnésium. Les études rapportent des carences fréquentes en raison des habitudes alimentaires. Le stress répété et l’anxiété peuvent être à l’origine d’une perte accrue de magnésium par l’organisme. La supplémentation en magnésium est une solution nutraceutique pour en couvrir les besoins, corriger les désordres liés à un apport insuffisant, à une malabsorption ou à une élimination trop importante.
Toutefois, face aux différentes formes de magnésium présentes sur le marché, il est parfois difficile de faire son choix… L’équipe scientifique du laboratoire Nutrixeal vous apporte dans ce dossier des éléments de compréhension indispensables pour comparer efficacement les étiquetages !
Consulter le dossier :
- Homéostasie du magnésium dans l’organisme
- Causes et symptômes d’un déficit en magnésium
- Supplémentation en magnésium : quelle(s) forme(s) choisir ?
- Cofacteurs nutraceutiques de la supplémentation en magnésium
- Conclusion
- Le choix Nutrixeal
- Références
Homéostasie du magnésium
dans l’organisme [1], [2]
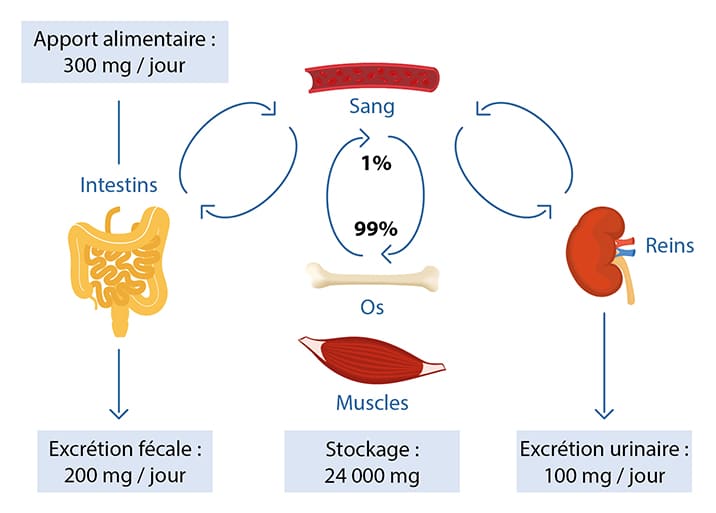
Le corps humain d’un adulte contient au total 22 à 26 grammes de magnésium. La majorité de ce magnésium se trouve dans le milieu intracellulaire (99%) alors qu’une très faible fraction occupe le milieu extracellulaire (1%). Ce magnésium est apporté par l’alimentation. Il est principalement stocké dans les os et les muscles. 30 à 40 % du magnésium provenant de l’alimentation sera absorbé par l’intestin, le reste étant excrété par le tube digestif. Le rein, quant à lui, assure une excrétion urinaire de magnésium. Les pertes de magnésium liées à la transpiration sont faibles mais peuvent devenir significatives en cas d’exercice physique intense. Dans des conditions physiologiques normales, un équilibre entre les apports alimentaires et les excrétions de magnésium permet d’assurer son homéostasie. Cependant des apports insuffisants ou une excrétion trop importante peuvent être à l’origine d’une carence en magnésium.
Causes et symptômes d’un déficit en magnésium
Causes d’un déficit en magnésium [3]
Un déficit en magnésium peut résulter d’un ou plusieurs mécanismes tels que des apports alimentaires insuffisants, une absorption digestive réduite ou une élimination excessive.

Apport alimentaire insuffisant :
Une étude a mis en évidence que l’apport alimentaire en magnésium était insuffisant dans la population française.
Ces apports seraient en-dessous des recommandations pour 77% des femmes et 72% des hommes. Aussi, pour 23% des femmes et 18% des hommes, les deux tiers des apports recommandés ne seraient pas atteints[4].

Absorption digestive réduite :
Des troubles digestifs chroniques tels que des diarrhées ou des vomissements peuvent être à l’origine d’une absorption réduite de magnésium, ces troubles ne permettant qu’une absorption partielle du bol alimentaire et donc du magnésium ingéré. Les maladies inflammatoires chroniques de l’intestin mais aussi des résections chirurgicales du tube digestif seraient également à l’origine d’hypomagnésémies.
Élimination rénale excessive :
Certaines mutations génétiques pourraient être à l’origine de déficits en magnésium, notamment sur des gènes codant pour des protéines assurant la réabsorption rénale du magnésium.
Médicaments :
De nombreux médicaments rapportent être à l’origine d’hypomagnésémies. Parmi ces médicaments figurent les IPP (inhibiteurs de la pompe à protons) utilisés comme traitement du reflux gastro-œsophagien ou comme traitement des ulcères gastro-duodénaux. La modification du pH du contenu digestif qu’il entraîne expliquerait une absorption réduite du magnésium. Des médicaments diurétiques seraient aussi à l’origine de déficits en magnésium par une excrétion urinaire accrue. D’autres médicaments tels que les laxatifs et certains immunosuppresseurs sont également rapportés comme hypomagnésémiants.
Stress :
Le stress présente la particularité d’être à la fois cause et conséquence d’un déficit en magnésium. Un stress ponctuel déclenche une sécrétion d’adrénaline conduisant à son tour à une libération du magnésium des tissus vers la circulation sanguine. Le rein filtrera une quantité de magnésium plus importante et son élimination urinaire sera alors majorée. Lors de stress répétés, la sécrétion de cortisol aboutit au même résultat quant à la fuite de magnésium vers les urines. Or, le déficit en magnésium a montré accroître la vulnérabilité face au stress. On parle alors de cercle vicieux stress/magnésium. Dans le monde moderne, l’éviction du stress étant souvent difficile à mettre en place, la supplémentation en magnésium représente une approche utile et intéressante dans la prise en charge du stress, ce qui est souligné dans de nombreuses études[5].
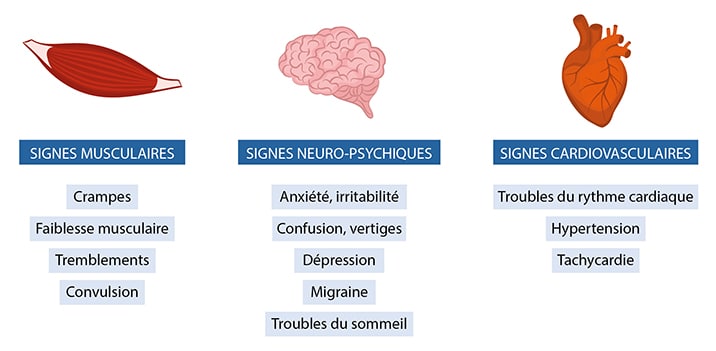
Symptômes de déficit en magnésium[6]
La plupart des signes cliniques évoquant un déficit en magnésium sont des troubles d’ordre neuro-psychique, musculaire ou cardiaque. Mais le déficit peut également être asymptomatique.
Pourquoi est-il difficile d’évaluer un déficit en magnésium en biologie médicale[7] ?
Seulement 1% du magnésium total du corps humain se trouve dans le milieu extracellulaire. Sa très faible concentration plasmatique est à l’origine d’une mesure ne reflétant pas le stock total de l’organisme. Une hypomagnésémie, c’est-à-dire une faible concentration de magnésium dans le plasma sanguin, traduira un déficit en magnésium avec une grande certitude. Cependant, il est fréquent qu’un déficit en magnésium soit présent, bien que la magnésémie soit satisfaisante.
Le dosage du magnésium intra-érythrocytaire serait plus qualitatif et représentatif des réserves en magnésium que le dosage plasmatique.
Un dosage de la magnésurie sur 24h, c’est-à-dire de la concentration en magnésium dans les urines, permet de préciser le diagnostic.
Par simplicité, le déficit en magnésium est généralement évalué par dosage plasmatique en 1ère intention.
Supplémentation en magnésium : quelle(s) forme(s) choisir ?[8]
Une supplémentation en magnésium peut s’avérer très utile en cas de manifestations cliniques d’un déficit, d’apports alimentaires insuffisants, d’absorption intestinale réduite ou d’élimination excessive. Le stress est une situation devant évoquer un déficit en magnésium. Différentes solutions nutraceutiques peuvent être envisagées et pour lesquelles l’absorption du magnésium peut être optimisée par le choix du sel, les conditions d’administration ou encore d’autres ingrédients nutraceutiques synergiques. Pour corriger un déficit avéré, une supplémentation de 3 à 6 mois est recommandée.
De nombreuses études rapportent les bienfaits du magnésium dans divers axes santé bien documentés tels que le stress, la sphère cognitive et les troubles musculaires mais aussi l’asthme, le diabète, l’ostéoporose ou encore le sevrage tabagique[9].
Magnésium : un traitement préventif de la migraine[10], [11], [12] ?
Un déficit en magnésium a été mis en évidence chez des patients migraineux. Ce déficit jouerait un rôle dans l’apparition des migraines notamment par l’induction d’une vasoconstriction artérielle cérébrale. Une étude rapporte une réduction de la fréquence des crises d’au moins 40% avec une supplémentation en magnésium ainsi qu’une diminution significative de la consommation de médicaments antimigraineux. Une autre étude rapporte également une réduction de la fréquence des crises avec une diminution de l’intensité de la douleur. La supplémentation en magnésium présenterait aussi un intérêt chez la femme en cas de migraines liées au cycle menstruel.
Comparaison des différents sels de magnésium :
Trois familles de sels de magnésium existent sur le marché. Il s’agit de magnésium sous différentes formes telles que les sels inorganiques, les sels organiques et les formes chélatées. En nutraceutique ces sels sont sélectionnés sur trois principaux critères : leur solubilité, leur biodisponibilité et leur tolérance digestive.
Formes de magnésium à éviter :
Les sels inorganiques insolubles (oxyde de magnésium, hydroxyde de magnésium, carbonate de magnésium), les sels inorganiques solubles (chlorure de magnésium et sulfate de magnésium) et certains sels organiques (lactate de magnésium et gluconate de magnésium) présentent un effet laxatif souvent prononcé[13].
L’oxyde de magnésium est un sel de magnésium souvent employé dans les compléments alimentaires et pourtant de nombreuses études le caractérisent comme un sel peu soluble, dont la biodisponibilité serait relativement faible. Les troubles digestifs qu’il entraîne sont relativement fréquents. Il présente cependant l’avantage d’un pourcentage élevé de magnésium élémentaire dans sa formule, ce qui facilite le conditionnement industriel en raison du faible encombrement qu’il occupe dans les formulations (gélules, comprimés, etc.). Mais ce sel ne relève aucunement d’une sélection de haute de qualité nutraceutique.
Et le magnésium marin ?
Les sels de magnésium d’origine marine présentent une bonne presse cependant aucune étude scientifique ne rapporte un intérêt nutraceutique d’une telle provenance. De plus, il s’agit souvent de magnésium sous forme oxydée, une forme de magnésium caractérisée par une faible solubilité et une tolérance intestinale limitée. Le magnésium marin sous forme d’oxydes de magnésium présente l’avantage d’être bon marché et de contourner les contraintes industrielles en raison d’une teneur en magnésium élément élevée, mais cette forme entraîne fréquemment des diarrhées.
Formes de magnésium conseillées :
Les formes chélatées de magnésium ainsi que certains sels organiques présentent une biodisponibilité supérieure aux sels inorganiques. La biodisponibilité est en général étroitement liée à la solubilité du sel de magnésium utilisé.
Le glycérophosphate de magnésium est un sel qui bénéficie d’une très haute solubilité et d’une tolérance intestinale maximale, permettant ainsi une très bonne biodisponibilité. Le glycérophosphate peut également constituer une source intéressante de phosphore et de glycérol. Les apports journaliers recommandés en phosphore sont de 700 mg par jour. Le phosphore présente un intérêt dans de nombreux axes santé, tels que le métabolisme énergétique, le développement osseux ou encore la dentition, et les phosphates sont des constituants essentiels à l’intégrité des membranes cellulaires. Le glycérol, quant à lui, représente un substrat énergétique intéressant pour l’organisme.
Le bisglycinate de magnésium correspond à une forme chélatée (par l’acide aminé glycine) disposant d’une haute solubilité. Cette forme de magnésium dispose d’une excellente absorption intestinale, en raison d’un mécanisme de transport spécifique et supplémentaire aux sels organiques et inorganiques. Cette absorption supplémentaire correspond à un transport par des canaux peptidiques (spécifiques des acides aminés), en plus des mécanismes d’absorption actifs et passifs. La glycine apportée par ce magnésium est également intéressante pour l’organisme. Il s’agit d’un acide aminé essentiel à la synthèse de nombreuses protéines, dont le collagène.
Moins connu, l’acétyl-taurinate de magnésium fait également partie des formes de magnésium bien tolérées et assimilées. Les propriétés lipophiles de l’acétyl-taurinate permettent à la molécule de traverser la barrière hémato-encéphalique, ce qui en fait un actif de choix pour la sphère cognitive[14], [15]. L’acétyl-taurinate étant une « grosse molécule », le pourcentage élémentaire en magnésium dans cet ingrédient est faible. Mais l’acétyl-taurinate de magnésium a une action propre, non-liée au simple apport de magnésium. La taurine contenue dans la molécule exerce un effet de neurotransmission (cf. paragraphe ci-après « Cofacteurs nutraceutiques de la supplémentation en magnésium ») qui se combine aux effets bénéfiques du magnésium. Les études ont ainsi montré que de petites doses étaient suffisantes pour obtenir les effets escomptés sur le système nerveux.
Parmi les sels d’assez bonne qualité nutraceutique, on retrouve également le citrate de magnésium, qui semble être relativement bien toléré sur le plan intestinal, avec une biodisponibilité correcte.
Des études scientifiques pas toujours concluantes
Mais alors, parmi les formes de magnésium à bonne tolérance intestinale, laquelle choisir ? Existe-t-il une forme supérieure aux autres en termes de biodisponibilité ? Pour répondre à cette question, il faudrait idéalement disposer d’une étude clinique comparative correctement construite, comparant dans les mêmes conditions l’absorption des différents sels de magnésium de bonne qualité (par mesure de l’excrétion urinaire et fécale de magnésium). Malheureusement, une telle étude n’existe pas à ce jour… Les études menées jusqu’à présent comparent généralement des oxydes de magnésium avec une ou parfois deux formes organiques, ce qui ne permet pas de conclure par rapport à l’ensemble des formes disponibles. Et les protocoles de ces études sont souvent discutables…
Gare également à la surinterprétation des résultats d’études ! A titre d’exemple, l’étude régulièrement mise en avant par certains auteurs pour étayer une prétendue supériorité du citrate de magnésium[16] comporte des biais méthodologiques rendant cette conclusion pour le moins hâtive. Dans ces travaux, les chercheurs ont mesuré l’excrétion urinaire de magnésium, mais pas l’excrétion fécale (paramètre tout aussi important). Le citrate de magnésium est ici comparé à des oxydes et à un magnésium chélaté aux acides aminés (MCAA). Les deux formes organiques obtiennent sans surprise des résultats bien supérieurs aux oxydes sur l’ensemble des paramètres mesurés. Toutefois, le citrate paraît mieux absorbé que le MCAA uniquement sur les teneurs en magnésium dans la salive et le sérum sanguin, qui comme nous l’avons expliqué plus haut, sont des paramètres peu représentatifs du statut en magnésium de l’organisme. Aucune différence significative n’est rapportée entre l’excrétion urinaire du citrate de magnésium et celle du MCAA.
Par conséquent, face à l’absence d’étude sérieuse et exhaustive sur le sujet, l’humilité et la rigueur scientifique dictent de ne pas distinguer de champion absolu et universel parmi les différentes formes de magnésium de « bonne qualité ». Néanmoins, dans certains cas particuliers, quelques formes de magnésium se distinguent, comme par exemple l’acétyl-taurinate de magnésium pour la sphère cognitive et le glycérophosphate de magnésium lorsqu’il s’agit d’ajouter du magnésium dans une boisson (cf. paragraphe ci-dessous).
Modalités d’administration du magnésium[2], [17] :
De nombreux éléments concernant les modalités d’administration du magnésium ont été mis en évidence comme favorisant son absorption.
Une supplémentation sous forme d’un sel solubilisé augmenterait l’absorption du magnésium. En ajout à une boisson, certains sels de magnésium peuvent être utilisés en raison de leur bonne solubilité.
Le bol alimentaire pourrait aussi influencer favorablement l’absorption du magnésium. La digestion permet un temps de contact prolongé du magnésium avec les muqueuses digestives. Une administration du magnésium au moment du repas pourrait donc en améliorer sa biodisponibilité.
Des nombreuses études ont également mis en évidence que la plupart des fibres pourraient augmenter l’absorption intestinale du magnésium ainsi qu’un fractionnement de la dose sur l’ensemble de la journée.
Une supplémentation en magnésium sous une forme à solubiliser dans l’eau et administrée de façon fractionnée à chaque repas de la journée réunirait toutes les conditions d’administration pour une assimilation maximale. Le glycérophosphate de magnésium permet de réunir facilement toutes ces conditions. Il bénéficie d’une absence de goût après mise en solution et d’une excellente solubilité indépendante du pH. Le bisglycinate présente une praticité moins élevée en raison d’un goût généralement inapprécié et une solubilité certes élevée, mais relativement plus sensible aux variations de pH du milieu digestif.
Cofacteurs nutraceutiques de la supplémentation en magnésium :
La vitamine B6 et le magnésium ont des activités étroitement liées. Ils interviennent en synergie dans de nombreux mécanismes biochimiques. La vitamine B6 intervient comme régulateur du système nerveux et favorise la captation du magnésium par les cellules de l’organisme.
La taurine est un acide aminé naturel présent sous forme libre dans de nombreux tissus. Le corps humain en assure une biosynthèse, afin notamment d’assurer la production d’acides biliaires. La taurine se retrouve également dans des aliments comme la viande, le poisson et les fruits de mer. Les huîtres et les noix de Saint-Jacques en contiennent respectivement 1200 mg et 600 mg pour 100 g [18]. On en retrouve aussi en quantité importante dans le lait maternel[19]. La taurine est impliquée dans plusieurs mécanismes biologiques, tels que la stabilisation des membranes cellulaires, la neuromodulation et la régulation des flux ioniques[20]. L’action de la taurine sur les récepteurs GABA favoriserait la rétention du magnésium par régulation du stress. On parle d’elle comme d’un « magnésio-fixateur ».
La taurine tient son nom du fait qu’elle ait été découverte dans la bile de taureau. Toutefois, la taurine utilisée par Nutrixeal n’est nullement d’origine animale. L’utilisation de cet acide aminé dans certaines boissons énergisantes lui a constitué à tort la réputation de substance excitante. Mais aucune étude scientifique ne rapporte d’action excitante ou stimulante après ingestion de taurine.
Conclusion
Le magnésium est un minéral indispensable au bon fonctionnement de l’organisme et son déficit est à l’origine de nombreuses manifestations cliniques. L’intérêt d’une supplémentation a été démontrée dans de multiples études. Le choix du sel de magnésium est déterminant en nutraceutique et doit reposer sur différents critères tel que sa solubilité, sa biodisponibilité et sa tolérance digestive.
Le choix Nutrixeal s’est porté sur 3 formes de magnésium de haute qualité :
Pour le complexe UltraMag® en gélules végétales, avec de la taurine et de la vitamine B6, Nutrixeal a choisi le bisglycinate de magnésium de qualité Albion TRAACS®, garanti 100% chélaté, sans oxydes de magnésium. Cette forme bénéficie d’un mécanisme d’absorption spécifique aux acides aminés, qui s’ajoute aux voies d’absorption classiques du magnésium. De plus, le bisglycinate constitue un apport de glycine intéressant pour l’organisme.

Et pour en savoir plus sur le fournisseur Albion® :
Pour les adeptes des boissons, le choix Nutrixeal s’est porté sur le glycérophosphate de magnésium (PhosphoMag®), pour ses excellentes qualités organoleptiques, bien meilleures que celles du bisglcycinate.
Enfin, pour la sphère cognitive, Nutrixeal a choisi l’acétyl-taurinate de magnésium, qui se distingue nettement dans ce domaine.
Auteurs
Dr. Florian Laracine, docteur en pharmacie
Dr. Mathilde Clier, PhD, docteur en biologie cellulaire
Références :
[1] J. W. Seo et T. J. Park (20008). Electrolyte Blood Press, vol. 6, no 2, p. 86‑95.
[2] J. P. Schuchardt et A. Hahn (2017). Curr Nutr Food Sci, vol. 13, no 4, p. 260‑278.
[3] J. Ayuk et N. J. L. Gittoes. (2014). Ann. Clin. Biochem., vol. 51, no Pt 2, p. 179‑188.
[4] P. Galan et al. (1997). Magnes Res, vol. 10, no 4, p. 321‑328.
[5] N. B. Boyle, C. Lawton, et L. Dye (2017). – A Systematic Review. Nutrients, vol. 9, no 5.
[6] J. J. DiNicolantonio, J. H. O’Keefe, et W. Wilson (2018). Open Heart, vol. 5, no 1, p. e000668.
[7] A. M. Badran et P. Crenn (2009). Nutrition Clinique et Métabolisme 23(1):9-15.
[8] S. Siebrecht (2013). International Journal of orthomolecular and related medicine, Nr. 144-2013.
[9] G. K. Schwalfenberg et S. J. Genuis (2017). Scientifica (Cairo), vol. 2017.
[10] E. Köseoglu, A. Talaslioglu, A. S. Gönül, et M. Kula (2008). Magnes Res, vol. 21, no 2, p. 101‑108.
[11] A. Peikert, C. Wilimzig, et R. Köhne-Volland (1996). Cephalalgia, vol. 16, no 4, p. 257‑263.
[12] F. Facchinetti, G. Sances, P. Borella, A. R. Genazzani, et G. Nappi (1991). Headache, vol. 31, no 5, p. 298‑301.
[13] F. C. M. Driessens, M. G. Boltong, et J. A. Planell (1993). Magnes Bull, p. 3.
[14] P. Bac, C. Herrenknecht, P. Binet, et J. Durlach (1993). Magnes Res, vol. 6, no 1, p. 11‑19.
[15] P. Bac, C. Herrenknecht, N. Pagès, C. Dupont, et J. Durlach (1996). Magnes Res, vol. 9, no 4, p. 281‑291.
[16] A. F. Walker, G. Marakis, S. Christie, et M. Byng (2003). Magnes Res, vol. 16, no 3, p. 183‑191.
[17] M. Sabatier et al. (2011). Br. J. Nutr., vol. 106, no 3, p. 331‑334.
[18] Y. Yamori, T. Taguchi, A. Hamada, K. Kunimasa, H. Mori, et M. Mori (2010). J Biomed Sci, vol. 17, no Suppl 1, p. S6.
[19] D. K. Rassin, J. A. Sturman, et G. E. Guall (1978). Dev., vol. 2, no 1, p. 1‑13.
[20] S. Schaffer et H. W. Kim (2018). Biomol Ther (Seoul), vol. 26, no 3, p. 225‑241.




🙂